解答题-工业流程题 适中0.65 引用0 组卷495
2020年初比亚迪汉EV和特斯拉Model 3均搭载了磷酸亚铁锂(LiFePO4)电池组。某企业设计了磷酸亚铁锂电池正极生产和回收的工艺流程如下:
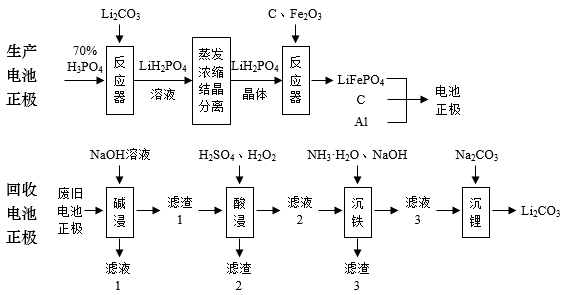
已知:①Ksp[Fe(OH)3]=10-39;②Li2CO3的溶解度:0°C为1.54g, 100°C为0.72g。
(1)反应釜中反应的化学方程式为_______ 。
(2)获得LiH2PO4,晶体的分离操作是_______ ,反应器中加入C的目的是_______ 。
(3)写出一条可以提高“碱浸”效率的措施_______ 。
(4)向滤液1中加入过量CO2可得到白色胶状物质,该反应的离子方式为_______ 。
(5)“酸浸”时若用HNO3代替H2O2,缺点是____ ,若“沉铁"后溶液中c(Fe2+)=10 -6mol·L-1,则该过程应调节pH=___ ,“ 沉锂”时,所得Li2CO3应选择___ (“冷水”或“热水")进行洗涤;从滤渣2中可以回收循环利用___ (填化学式)。

已知:①Ksp[Fe(OH)3]=10-39;②Li2CO3的溶解度:0°C为1.54g, 100°C为0.72g。
(1)反应釜中反应的化学方程式为
(2)获得LiH2PO4,晶体的分离操作是
(3)写出一条可以提高“碱浸”效率的措施
(4)向滤液1中加入过量CO2可得到白色胶状物质,该反应的离子方式为
(5)“酸浸”时若用HNO3代替H2O2,缺点是
类题推荐
磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。废旧电池正极片(磷酸亚铁锂、炭黑和铝箔等)可再生利用,其工艺流程如图:
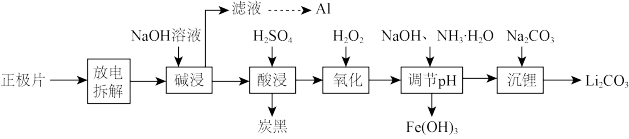
已知:碳酸锂在水中的溶解度:0℃时1.54g,90℃时0.85g,100℃时0.71g。
(1)上述流程中要得到Li2CO3的操作是____________________ 。
(2) “氧化”发生反应的离子方程式为________________ ;若用HNO3代替H2O2,不足之处是______ 。
(3)①已知Ksp[Fe(OH)3]=2.6×10-39。常温下,在Fe(OH)3悬浊液中,当溶液的pH=3.0时,Fe3+的浓度为________ mol·L-1。
②“调节pH”生成沉淀时,溶液pH与金属元素的沉淀百分率(ω)的关系如表:
则最佳的沉淀pH=_______ 。
(4) “沉锂”时所得的沉淀应用_______ 洗涤(填“热水”或“冷水”)。
(5)甲醇燃料电池在工作时,正极发生反应的物质是______ ,该电池在酸性条件放电时正极的电极反应式为___________________ 。

已知:碳酸锂在水中的溶解度:0℃时1.54g,90℃时0.85g,100℃时0.71g。
(1)上述流程中要得到Li2CO3的操作是
(2) “氧化”发生反应的离子方程式为
(3)①已知Ksp[Fe(OH)3]=2.6×10-39。常温下,在Fe(OH)3悬浊液中,当溶液的pH=3.0时,Fe3+的浓度为
②“调节pH”生成沉淀时,溶液pH与金属元素的沉淀百分率(ω)的关系如表:
| pH | 3.5 | 5.0 | 6.5 | 8.0 | 10.0 | 12.0 |
| ω(Fe)/% | 66.5 | 79.2 | 88.5 | 97.2 | 97.4 | 98.1 |
| ω(Li)/% | 0.9 | 1.3 | 1.9 | 2.4 | 4.5 | 8.0 |
则最佳的沉淀pH=
(4) “沉锂”时所得的沉淀应用
(5)甲醇燃料电池在工作时,正极发生反应的物质是
2019年诺贝尔化学奖授予约翰·古迪纳夫、斯坦利·威廷汉和吉野彰,表彰他们对锂离子电池研究的贡献。磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。采用湿法治金工艺回收废旧磷酸亚铁锂电池正极片(除LiFePO4外,还含有Al箔、少量不溶于酸碱的导电剂)中的资源,部分流程如图:
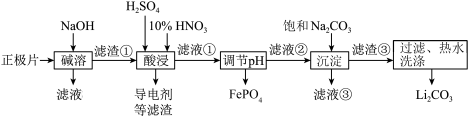
已知:Ksp ( Li2CO3)=1.6×10-3。部分物质的溶解度(S)如下表所示:
(1)从“正极”可以回收的金属有___ 。
(2)写出碱溶时Al箔溶解的离子方程式___ 。
(3)磷酸亚铁锂电池在工作时,正极发生LiFePO4和FePO4的转化,该电池充电时正极的电极反应式为___ 。
(4)酸浸时产生标准状况下3.36LNO时,溶解 LiFePO4___ mol(其他杂质不与HNO3反应),若用H2O2代替HNO3,发生反应的离子方程式为___ 。
(5)流程中用“热水洗涤”的原因是___ 。
(6)若滤液②中c(Li+)=4mol/L,加入等体积的Na2CO3后,Li+的沉降率到90%,计算滤液③中c(CO32-)=___ mol/L。
(7)“沉淀”时___ (填“能”或“不能”)用Na2SO4溶液代替饱和Na2CO3溶液,原因是___ 。

已知:Ksp ( Li2CO3)=1.6×10-3。部分物质的溶解度(S)如下表所示:
| T℃ | S(Li2CO3)/g | S(Li2SO4)/g | S(Li3PO4)/g |
| 20 | 1.33 | 34.2 | 0.039 |
| 80 | 0.85 | 30.5 | —— |
| 100 | 0.72 | —— |
(1)从“正极”可以回收的金属有
(2)写出碱溶时Al箔溶解的离子方程式
(3)磷酸亚铁锂电池在工作时,正极发生LiFePO4和FePO4的转化,该电池充电时正极的电极反应式为
(4)酸浸时产生标准状况下3.36LNO时,溶解 LiFePO4
(5)流程中用“热水洗涤”的原因是
(6)若滤液②中c(Li+)=4mol/L,加入等体积的Na2CO3后,Li+的沉降率到90%,计算滤液③中c(CO32-)=
(7)“沉淀”时
磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。废旧电池正极片(磷酸亚铁锂、炭黑和铝箔等)可再生利用,其工艺流程如图:
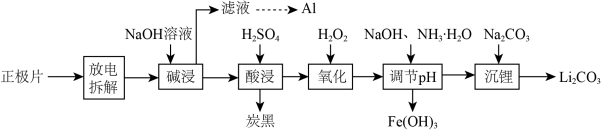
已知:碳酸锂在水中的溶解度:0℃时1.54g,90℃时0.85g,100℃时0.71g。
(1)上述流程中要得到Li2CO3的操作是___ 。
(2) “氧化”发生反应的离子方程式为___ ;若用HNO3代替H2O2,不足之处是___ 。
(3)①已知Ksp[Fe(OH)3]=2.6×10-39。常温下,在Fe(OH)3悬浊液中,当溶液的pH=3.0时,Fe3+的浓度为___ mol·L-1。
②“调节pH”生成沉淀时,溶液pH与金属元素的沉淀百分率(ω)的关系如表:
则最佳的沉淀pH=___ 。
(4) “沉锂”时所得的沉淀应用___ 洗涤(填“热水”或“冷水”)。
(5)磷酸亚铁锂电池在工作时,正极发生LiFePO4和FePO4的转化,该电池放电时正极的电极反应式为___ 。

已知:碳酸锂在水中的溶解度:0℃时1.54g,90℃时0.85g,100℃时0.71g。
(1)上述流程中要得到Li2CO3的操作是
(2) “氧化”发生反应的离子方程式为
(3)①已知Ksp[Fe(OH)3]=2.6×10-39。常温下,在Fe(OH)3悬浊液中,当溶液的pH=3.0时,Fe3+的浓度为
②“调节pH”生成沉淀时,溶液pH与金属元素的沉淀百分率(ω)的关系如表:
| pH | 3.5 | 5.0 | 6.5 | 8.0 | 10.0 | 12.0 |
| ω(Fe)/% | 66.5 | 79.2 | 88.5 | 97.2 | 97.4 | 98.1 |
| ω(Li)/% | 0.9 | 1.3 | 1.9 | 2.4 | 4.5 | 8.0 |
则最佳的沉淀pH=
(4) “沉锂”时所得的沉淀应用
(5)磷酸亚铁锂电池在工作时,正极发生LiFePO4和FePO4的转化,该电池放电时正极的电极反应式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


